BIOALLIANCE PHAR: pourrait se réveillerBIOALLIANCE PHARMA : pourrait se réveiller
2007-10-12 | Actualités sociétés
La semaine qui s’achève aura été incontestablement favorable au secteur des biotecths. Après
une séance de lundi réservée au rattrapage du titre CEREP, largement abandonné depuis de longues
semaines… la séance de mardi a vu le mouvement d’intérêt se porter sur TRANSGENE, puis
mercredi sur EXONHIT, avant que nous assistions ce jeudi à un regain d’investissement sur le
titre INNATE.
BIOALLIANCE PHARMA qui détient tous les ingrédients propices à une plus juste valorisation,
finira t elle par attirer les investisseurs afin de revenir à un niveau de valorisation plus
équitable.
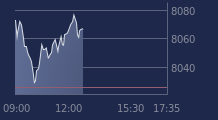
Nous estimons que le cours de valeur pourrait inciter le marché à s’investir sur le titre. Nous
ne modifions en aucun cas notre objectif de 16 euros. A 11.14 euros rien ne devrait nous retenir
pour opérer un investissement profitable.
T3 le 26/10
http://www.bioalliancepharma.com/investors.asp
http://www.euroland-finance.com/analyses/clients/071/2007-07-04_09_00_Newsletter_4_Juillet_2007.pdf
BioAlliance Pharma : Accord US de licensing pour le Loramyc® 12,28 €
Specialty Pharma Eurolist C
Conf Call
BioAlliance Pharma vient de signer avec PAR Pharmaceutical Companies
Inc. un accord de licensing pour la commercialisation aux USA du Loramyc
® développé dans le traitement des candidoses oropharyngées
chez les patients immunodéprimés (VIH, cancers) . Dans le cadre de cet
accord exclusif, BioAlliance Pharma perçoit un upfront payment de 15
M$ et jusqu’à 50 M$ en milestones (répartis en 20 M$ pour l’enregistrement
à la FDA et 30 M$ pour l’atteinte de seuils de CA du Loramyc®). Des
royalties progressives seront également perçues dès la commercialisation
aux USA. Compte tenu de la taille du marché des candidoses oropharyngées,
nous estimons que le taux progressif de royalties devrait se situer,
selon 2 tranches de CA, entre 12-15% puis 18-20%. Notre peak sales aux
USA étant évalué à 55 M€ (sur la base d’un coût de traitement journalier
de 8$), nous anticipons que le seuil de progression des royalties devrait
être autour des 30 M€ de ventes réalisées par PAR Pharmaceutical. Le
miconazole Lauriad® est en cours d’essai de phase III visant à inclure 540
patients (USA, Canada, Afrique du Sud). La fin du recrutement est attendue
pour le T4 2007 pour un lancement aux USA en 2009.
Cet accord s’inscrit dans le plan de développement et de commercialisation
du Loramyc®, après la création de la JV 50/50 « SpeBio » signée
avec SpePharm pour l’Europe (ex-France). PAR Pharmaceutical Companies
Inc. (Nyse : PRX — Capi. : $ 1,30 Md) développe et commercialise
des génériques ainsi que des spécialités pharmaceutiques destinées à
des marchés de niche. Avec plus d’une vingtaine d’accords de licensing,
PAR Pharmaceutical commercialise déjà une large gamme de génériques
dans les pathologies infectieuses comme le fluconazole utilisé dans
les traitement des candidoses. Présent avec Megace® ES dans l’immunodépression
chez les patients atteints par le VIH (traitement de l’anorexie/
cachexie induite), une force de vente dédiée de +100 visiteurs médicaux
sera également chargée de la promotion du Loramyc® en oncologie,
médecine interne et auprès des professionnels paramédicaux.
EuroLand Finance
Focus BioSciences
7
Dans les prochaines étapes de lancement du Loramyc®, BioAlliance
Pharma est en cours d’investigation pour trouver à moyen-terme un partenaire
ad-hoc sur l’Asie.
Conseil :
Cet accord US de licensing s’inscrit dans un plan de lancement du Loramyc
® qui nous semble allier une approche pragmatique pour trouver le
partenariat ad-hoc (licensing US, JV Europe ex-France) sur un marché de
niche. L’excellente couverture de prescriptions et une anticipation
suffisante pour mener à bien la fin du développement clinique,
l’enregistrement et la formation de la force de vente de PAR
Pharmaceutical devrait permettre le lancement en 2009 aux USA . Nous
sommes très confiant sur la capacité du management à implémenter le
lancement du produit late-stage, le Loramyc® qui devrait assurer des
revenus bien identifiés à court-terme par le licensing US et la JV en Europe
ainsi que les ventes directes permettant l’avancement des autres
produits early-stage du pipeline. Nous avons un avis fondamental positif
sur le business model et les technologies de drug delivery de BioAlliance
Pharma. Nous initierons la couverture au T3.
(Gérard Pontonnier)